Come Studiarlo
- Home
- Razionale
- Stress Ossidativo
- Come Studiarlo
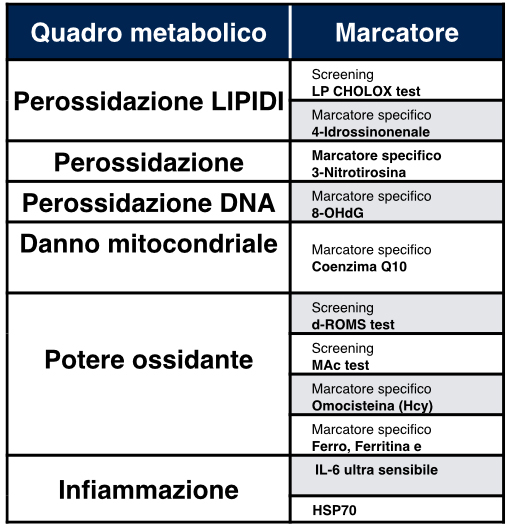
Studiare lo Stress Ossidativo
L’ossigeno è una molecola essenziale per la sopravvivenza degli organismi aerobi, come quello del uomo e di tutti gli animali; a causa della sua struttura atomica che non gli permette di accettare doppietti elettronici, esso può generare intermedi altamente instabili noti come radicali liberi o più propriamente specie reattive dell’ossigeno ROS.
Accanto ad essi, esiste un’analoga famiglia di radicali liberi, che hanno come protagonista l’azoto (simbolo N) invece dell’ossigeno, le cosiddette specie reattive dell’azoto RNS che svolgono a livelli fisiologici un’importante funzione di messaggeri intracellulari.
L’analisi diretta dei radicali liberi, sia ROS che RNS, è estremamente difficile a causa della loro elevata reattività e breve emivita: lo studio dello Stress Ossidativo si avvale, perciò, di analisi di laboratorio molto raffinate in grado di rilevare le alterazioni da essi indotte su proteine, lipidi e DNA.
Nello stesso tempo, vi è la possibilità di studiare le molecole che compongono la cosiddetta “barriera antiossidante”, composta da enzimi, vitamine ed altri riducenti che neutralizzando la formazione dei radicali garantiscono il più fisiologico equilibrio REDOX. Sebbene più soggette alle interferenze della dieta, anche le diminuzioni delle molecole con potere antiossidante, quali vitamine lipo- ed idro-solubili ed altre sostanze endogene riducenti come il glutatione (GSH) sono considerate marcatori indiretti di Stress Ossidativo.
ROS e RNS
I ROS comprendono tutti gli intermedi molecolari che con successive riduzioni monoelettroniche causano la trasformazione dell’ossigeno molecolare in acqua (H2O).
Possono essere suddivisi in due categorie:
- radicali liberi dell’ossigeno, anione superossido, radicale idrossile, ossigeno singoletto, contenenti un elettrone spaiato;
- specie non radicaliche (acqua ossigenata o perossido di idrogeno H2O2).
L’anione superossido è il primo radicale che si forma:
- per interazione dell’ossigeno con gli elettroni che talora sfuggono alla catena respiratoria quando questa funziona a regimi elevati, soprattutto nel passaggio REDOX da coenzima Q ai citocromi;
- nel corso di ossidazioni metallo dipendenti di molecole come adrenalina, noradrenalina e composti tiolici;
- per produzione diretta in alcune reazioni enzimatiche specifiche quali quelle catalizzate dalle xantino-ossidasi, triptofano diossigenasi e indolamine diossigenasi.
Le cellule infiammatorie producono grandi quantità di anione superossido come meccanismo di difesa contro batteri, virus e sostanze esogene: la dismutazione (trasformazione) dell’anione superossido a perossido di idrogeno (H2O2) può essere spontanea o catalizzata dalla superossido dismutasi (SOD).
Il perossido di idrogeno (H2O2) è una molecola reattiva relativamente stabile in grado di oltrepassare le membrane cellulari. Si può formare anche in alcune reazioni enzimatiche a livello di alcune particelle subcellulari, come i microsomi, i perossisomi e i mitocondri. E’ considerato un agente debolmente ossidante la cui tossicità risiede nella capacità di generare il radicale idrossile in reazioni enzimatiche catalizzate da ioni metallici.
Il radicale idrossile (HO-) è una molecola altamente reattiva con forti capacità ossidanti e costituisce l’agente principalmente responsabile della fase iniziale dei processi perossidativi nei tessuti. Si forma in reazioni catalizzate da ioni metallici, specie ferrosi, quando ad esempio il ferro, che è normalmente legato a proteine di trasporto e di deposito, transferrina e ferritina, si trova in uno stato libero.
L’ossigeno singoletto (1O2) è una forma di ossigeno altamente reattivo in grado di ossidare direttamente molte molecole organiche inclusi lipidi di membrana, aminoacidi, nucleotidi, carboidrati e tioli. Si forma tanto per esposizione alla luce ultravioletta quanto per attivazione dei macrofagi: l’azione della NADPH ossidasi produce il radicale anione superossido.
Le specie reattive dell’azoto RNS si formano quando elevati livelli endocellulari di anione superossido e perossido di idrogeno reagiscono con l‘ossido nitrico (NO). Questo radicale, che normalmente si forma a partire dall’aminoacido L-arginina in una reazione catalizzata dalla Ossido Nitrico Sintetasi (NOS) svolge in condizioni fisiologiche una fondamentale azione di messaggero intracellulare.
La sua reazione con anione superossido e perossido di idrogeno porta alla formazione di perossinitrito (OONO-) altamente citotossico con potere ossidante superiore di quello degli stessi ROS che lo hanno generato.
Biomarcatori di ossidazione delle proteine
Il processo di ossidazione delle proteine comporta generalmente l’introduzione di nuovi gruppi funzionali che possono contribuire ad alterarne la funzione ed il metabolismo. Il destino delle molecole alterate è generalmente la degradazione da parte del proteosoma o dei lisosomi, ma in alcuni casi si formano aggregati che si accumulano all’esterno della cellula e sono insensibili alla degradazione.
Biomarcatori di ossidazione dei lipidi
I fosfolipidi di membrana e i trigliceridi nelle LDL sono particolarmente suscettibili all’attacco dei radicali liberi. Gli idroperossidi lipidici che originano da una prima reazione che causa il riarrangiamento molecolare a livello dei doppi legami, sono a loro volta specie reattive che possono ulteriormente reagire a formare perossidi ciclici ed aldeidi alfa-beta-insature come la malondialdeide (MDA) e la 4-idrossi-nonenale (4-HNE). Poichè idroperossidi ciclici ed aldeidi possono essere assorbiti anche con la dieta, la misura di queste specie costituisce un buon indice di lipoperossidazione solo in presenza di uno stretto controllo del regime alimentare.
Biomarcatori di ossidazione del DNA
L’attacco dei ROS, in particolare del radicale idrossile (HO-), sugli acidi nucleici può causare mutazioni su specifiche basi e anche rottura della doppia elica. Il marcatore di danno ossidativo sul DNA più utilizzato è la 8-idrossi-deossi guanosina (8-OHdG). Durante il processo di riparazione in vivo del DNA e soprattutto in seguito alla degradazione degli acidi nucleici conseguente alla morte cellulare, la 8-OHdG viene liberata e secreta nelle urine, sia come base singola sia inclusa in oligomeri di DNA senza ulteriori modifiche. Data la stabilità e la specificità, la concentrazione di 8-OHdG nelle urine è uno dei più affidabili marcatori per valutare il grado di Stress Ossidativo sistemico.
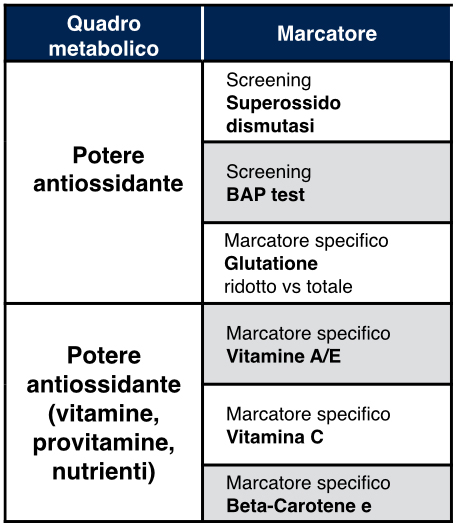
Potere antiossidante
Esistono in vivo sistemi enzimatici (superossidodismutasi, catalasi, perossidasi, reduttasi) e non enzimatici endogeni (antiossidanti a basso peso molecolare quali glutatione, NADH, acido urico, melatonina, acido alfa-lipoico) ed esogeni (vitamine A, E, C, chinoni, polifenoli) in grado di contrastare fisiologicamente ROS e RNS. Lo Stress Ossidativo ed i suoi effetti patologici intervengono nel momento in cui il rapporto di produzione dei radicali e loro neutralizzazione si sbilancia a favore dei primi.
Iscriviti alla newsletter
© Casa di Cura Privata Villa Margherita S.r.l. 2021
Designed by Teslathemes, Supported by WPmatic